EQUIPO 3...
NÚCLEO
El
núcleo atómico es la parte central de un
átomo, tiene
carga positiva, y concentra más del 99,9% de la masa total del átomo.
Está formado por
protones y
neutrones (denominados
nucleones) que se mantienen unidos por medio de la
interacción nuclear fuerte, la cual permite que el núcleo sea estable, a pesar de que los protones se repelen entre sí (como los polos iguales de dos
imanes). La cantidad de protones en el núcleo (
número atómico), determina el
elemento químico al que pertenece. Los núcleos atómicos no necesariamente tienen el mismo número de neutrones, ya que átomos de un mismo elemento pueden tener
masas diferentes, es decir son
isótopos del elemento.
La existencia del núcleo atómico fue deducida del
experimento de Rutherford, donde se bombardeó una lámina fina de oro con
partículas alfa, que son núcleos atómicos de
helio emitidos por rocas radiactivas. La mayoría de esas partículas traspasaban la lámina, pero algunas rebotaban, lo cual demostró la existencia de un minúsculo núcleo atómico.

Núcleo atómico
Para otros usos de este término, véase
Núcleo.
Representación aproximada del átomo de Helio. en el núcleo los protones están representados en rojo y los neutrones en azul. En la realidad el núcleo también es simétricamente esférico.
La
radiactividad o
radioactividad1 es un fenómeno físico por el cual los
núcleos de algunos
elementos químicos, llamados radiactivos, emiten
radiaciones que tienen la propiedad de impresionar placas radiográficas,
ionizar gases, producir
fluorescencia, atravesar cuerpos opacos a la luz ordinaria, entre otros. Debido a esa capacidad, se les suele denominar
radiaciones ionizantes (en contraste con las
no ionizantes). Las radiaciones emitidas pueden ser electromagnéticas, en forma de
rayos X o
rayos gamma, o bien corpusculares, como pueden ser
núcleos de helio,
electrones o positrones,
protones u otras. En resumen, es un fenómeno que ocurre en los núcleos de ciertos elementos inestables, que son capaces de transformarse o decaer, espontáneamente, en núcleos atómicos de otros elementos más estables.
La radiactividad
ioniza el medio que atraviesa. Una excepción la constituye el
neutrón, que posee carga neutra (igual carga positiva como negativa), pero ioniza la
materia en forma indirecta. En las desintegraciones radiactivas se tienen varios tipos de radiación:
alfa,
beta,
gamma y
neutrones libres.
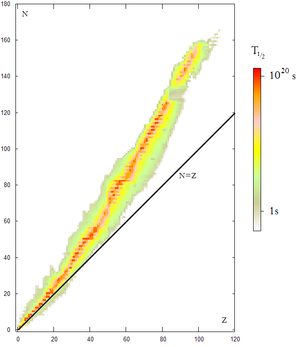
Diagrama de
Segrè. El color indica el
periodo de semidesintegración de los isótopos radiactivos conocidos, también llamado
semivida. Observe que un ligero exceso de neutrones favorece la estabilidad en átomos pesados.
La radiactividad
ioniza el medio que atraviesa. Una excepción la constituye el
neutrón, que posee carga neutra (igual carga positiva como negativa), pero ioniza la
materia en forma indirecta. En las desintegraciones radiactivas se tienen varios tipos de radiación:
alfa,
beta,
gamma y
neutrones libres.
La radiactividad es una propiedad de los
isótopos que son "inestables", es decir, que se mantienen en un
estado excitado en sus capas electrónicas o nucleares, con lo que, para alcanzar su
estado fundamental, deben perder energía. Lo hacen en emisiones electromagnéticas o en emisiones de partículas con una determinada
energía cinética. Esto se produce variando la energía de sus electrones (emitiendo
rayos X) o de sus
nucleones (rayo gamma) o variando el isótopo (al emitir desde el núcleo
electrones,
positrones, neutrones,
protones o partículas más pesadas), y en varios pasos sucesivos, con lo que un isótopo pesado puede terminar convirtiéndose en uno mucho más ligero, como el
uranio que, con el transcurrir de los siglos, acaba convirtiéndose en
plomo.
La radiactividad puede ser:
- Natural: manifestada por los isótopos que se encuentran en la naturaleza.
- Artificial o inducida: manifestada por los radioisótopos producidos en transformaciones artificiales.

Diagrama de Segrè indicando el tipo de decaimiento más probable.
CLASES Y
COMPORTAMIENTOS DE LA
RADIACTIVIDAD
Se comprobó que la radiación puede ser de tres clases diferentes, conocidas como partículas, desintegraciones y radiación:
- Partícula alfa: Son flujos de partículas cargadas positivamente compuestas por dos neutrones y dos protones (núcleos de helio). Son desviadas por campos eléctricos y magnéticos. Son poco penetrantes, aunque muy ionizantes. Son muy energéticas. Fueron descubiertas por Rutherford, quien hizo pasar partículas alfa a través de un fino cristal y las atrapó en un tubo de descarga. Este tipo de radiación la emiten núcleos de elementos pesados situados al final de latabla periódica (masa A >100). Estos núcleos tienen muchos protones y la repulsión eléctrica es muy fuerte, por lo que tienden a obtener N aproximadamente igual a Z (número atómico), y para ello se emite una partícula alfa. En el proceso se desprende mucha energía, que se convierte en la energía cinética de la partícula alfa, por lo que estas partículas salen con velocidades muy altas.
- Desintegración beta: Son flujos de electrones (beta negativas) o positrones (beta positivas) resultantes de la desintegración de los neutrones o protones del núcleo cuando este se encuentra en un estado excitado. Es desviada por campos magnéticos. Es más penetrante, aunque su poder de ionización no es tan elevado como el de las partículas alfa. Por lo tanto, cuando un átomo expulsa una partícula beta, su número atómico aumenta o disminuye una unidad (debido al protón ganado o perdido). Existen tres tipos de radiación beta: la radiación beta-, que consiste en la emisión espontánea de electrones por parte de los núcleos; la radiación beta+, en la que un protón del núcleo se desintegra y da lugar a un neutrón, a un positrón o partícula Beta+ y un neutrino, y por último la captura electrónica que se da en núcleos con exceso de protones, en la cual el núcleo captura un electrón de la corteza electrónica, que se unirá a un protón del núcleo para dar un neutrón.
- Radiación gamma: Se trata de ondas electromagnéticas. Es el tipo más penetrante de radiación. Al ser ondas electromagnéticas de longitud de onda corta, tienen mayor penetración y se necesitan capas muy gruesas de plomou hormigón para detenerlas. En este tipo de radiación el núcleo no pierde su identidad, sino que se desprende de la energía que le sobra para pasar a otro estado de energía más baja emitiendo los rayos gamma, o sea fotones muy energéticos. Este tipo de emisión acompaña a las radiaciones alfa y beta. Por ser tan penetrante y tan energética, éste es el tipo más peligroso de radiación.
- Cuando un átomo radiactivo emite una partícula alfa, la masa del átomo (A) resultante disminuye en 4 unidades y el número atómico (Z) en 2.
- Cuando un átomo radiactivo emite una partícula beta, el número atómico (Z) aumenta o disminuye en una unidad y la masa atómica (A) se mantiene constante.
- Cuando un núcleo excitado emite radiación gamma, no varía ni su masa ni su número atómico: sólo pierde una cantidad de energía hν (donde "h" es la constante de Plancky "ν" es la frecuencia de la radiación emitida).
Las dos primeras leyes indican que, cuando un átomo emite una radiación alfa o beta, se transforma en otro átomo de un elemento diferente. Este nuevo elemento puede ser radiactivo y transformarse en otro, y así sucesivamente, con lo que se generan las llamadas
series radiactivas.
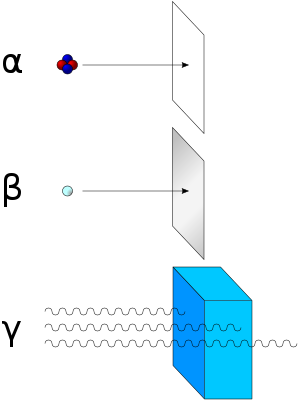
Clases de radiación ionizante y cómo detenerla.
Las partículas alfa (núcleos de helio) se detienen al interponer una hoja de papel. Las partículas beta (electrones y positrones) no pueden atravesar una capa de aluminio. Sin embargo, los rayos gamma (fotones de alta energía) necesitan una barrera mucho más gruesa, y los más energéticos pueden atravesar el plomo.
PROBLEMAS RESUELTOS
En una muestra de madera de un sarcófago ocurren 13536 desintegraciones en un día por cada gramo, debido al 14C presente, mientras que una muestra actual de madera análoga experimenta 920 desintegraciones por gramo en una hora. El período de semidesintegración del 14C es de 5730 años.
a) Establezca la edad del sarcófago.
b) Determine la actividad de la muestra del sarcófago dentro de 1000 años.
Solución:
a) Hay que pasar los dos datos de actividad a desintegraciones por segundo. En ambos casos el dato ofrecido es por gramo de muestra, por tanto, en el caso de la muestra del sarcófago:
Para el caso de la muestra actual la actividad se puede considerar como actividad en el instante inicial pues es un trozo de madera es de las mismas características a la del sarcófago:
Por otra parte, con el dato de T1/2 podemos conocer la constante de desintegración del carbono-14:
De la expresión de la actividad todo es conocido y podemos obtener el tiempo transcurrido:
t = 1’276 · 1011 s = 4045 años.
b) Dentro de 1000 años (1000 x 365’25 x 86400 = 3’156 · 107 s) el sarcófago tendrá una antigüedad de 5045 años (1’592 · 1011 s). Su actividad será de
* Tenemos 70 gramos del isótopo radiactivo cromo-51 (artificial), con un periodo de semidesintegración de 27 días. ¿Cuántos átomos quedarán de dicho isótopo al cabo de seis meses?
Solución
Con el dato del periodo de semidesintegración obtenemos la constante de desintegración del cromo-51:
Por otra parte, 70 gramos de cromo-51 son
Tenemos ya todos los datos necesarios para calcular el número de átomos que quedarán al cabo de seis meses (6 x 10 x 86400 = 1’56 · 107 s)
 La radiactividad o radioactividad1 es un fenómeno físico por el cual los núcleos de algunos elementos químicos, llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas radiográficas, ionizar gases, producirfluorescencia, atravesar cuerpos opacos a la luz ordinaria, entre otros. Debido a esa capacidad, se les suele denominarradiaciones ionizantes (en contraste con las no ionizantes). Las radiaciones emitidas pueden ser electromagnéticas, en forma de rayos X o rayos gamma, o bien corpusculares, como pueden ser núcleos de helio, electrones o positrones,protones u otras. En resumen, es un fenómeno que ocurre en los núcleos de ciertos elementos inestables, que son capaces de transformarse o decaer, espontáneamente, en núcleos atómicos de otros elementos más estables.
La radiactividad o radioactividad1 es un fenómeno físico por el cual los núcleos de algunos elementos químicos, llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas radiográficas, ionizar gases, producirfluorescencia, atravesar cuerpos opacos a la luz ordinaria, entre otros. Debido a esa capacidad, se les suele denominarradiaciones ionizantes (en contraste con las no ionizantes). Las radiaciones emitidas pueden ser electromagnéticas, en forma de rayos X o rayos gamma, o bien corpusculares, como pueden ser núcleos de helio, electrones o positrones,protones u otras. En resumen, es un fenómeno que ocurre en los núcleos de ciertos elementos inestables, que son capaces de transformarse o decaer, espontáneamente, en núcleos atómicos de otros elementos más estables.

No hay comentarios:
Publicar un comentario